2017-01-13
1、国产保健食品批文转让需要什么条件?
转让方和受让方需要满足一定条件才能进行保健食品批文转让。其中,受让方需要拥有经过GMP认证过的生产车间,各省市的认证种类和要求有所不同,具体可以咨询当地省局。
转让方
《保健食品批准证书》
受让方
(1)省级保健食品生产监督管理部门出具的受让方的保健食品卫生许可证复印件。
(2)省级保健食品生产监督管理部门出具的受让方符合《保健食品良好生产规范》的证明文件(《保健食品GMP证书》)。
2、保健食品批文转让需要多少时间?
保健食品批文转让需要通过保健食品技术转让注册申请最终获得新的保健食品批准证书。按照现行法规以及技术转让网统计数据,平均时间需要一年半时间。部分产品可在一年内完成。
3、什么样的保健食品需要补做试验?
对原料和主要辅料相同、口味或颜色不同的保健食品,如在新产品注册时未开展安全性毒理学评价试验和功能学评价试验,申请人在申请技术转让产品注册时,应当补做该两类试验。
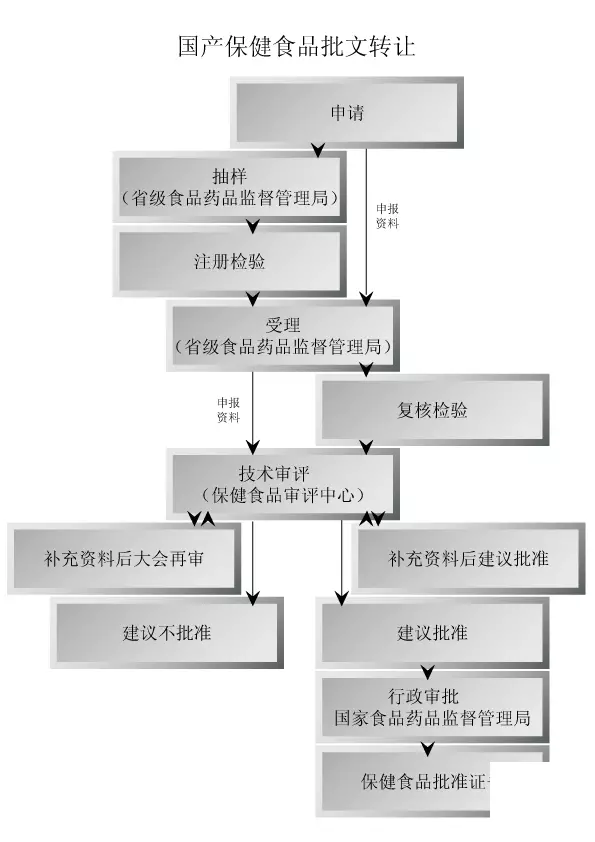
4、国产保健食品的转让流程是什么?
(一)签订合同:
受让方与转让方签订保健食品技术转让合同,并进行公证。
(二)生产样品:
受让方根据转让方提供的保健食品技术内容,生产保健食品技术转让检验用样品。
(三)样品检验:
根据保健食品技术转让检验要求,在国家食品药品监督管理总局指定的检验机构进行样品检验。
(四)递交申请材料:
申请人向受让方所在地的省级食品药品监督管理部门递交保健食品技术转让申请材料。
(五)提交补充资料:
收到国家食品药品监督管理总局的补充资料通知后,申请人应当在收到补充资料通知书后的5个月内提交符合要求的补充资料,未按规定时限提交补充资料的予以退审。特殊情况,不能在规定时限内提交补充资料的,必须向国家食品药品监督管理局提出书面申请,并说明理由。
(六)领取保健食品批准证书:
收到SFDA行政受理服务中心的保健食品批准证书领取通知后,申请人可自行于SFDA行政受理服务中心领取保健食品批准证书,或由CFDA行政受理服务中心寄出。
5、国产保健食品需要递交哪些资料?
(一)保健食品技术转让产品注册申请表。
(二)身份证、营业执照或者其它机构合法登记证明文件的复印件。
(三)经公证机关公证的转让方和受让方双方签订的有效转让合同。
(四)省级保健食品生产监督管理部门出具的受让方的保健食品卫生许可证复印件。
(五)省级保健食品生产监督管理部门出具的受让方符合《保健食品良好生产规范》的证明文件。
(六)保健食品批准证明文件原件(包括保健食品批准证书及其附件和保健食品变更批件)。
(七)受让方生产的连续三个批号的样品,其数量为检验所需量三倍。
