特殊医学用途配方食品注册办法详解
2016-06-06
国家食品药品监督管理总局颁布的《特殊医学用途配方食品注册管理办法》将于2016年7月1日正式实施,特殊医学用途配方食品的申报、生产、流通都将被规范管理。
《办法》中规定,只有具备以下全部条件的企业,才能有资质生产并申请注册特殊医学用途配方食品:
(1)具备所生产特殊医学用途配方食品相适应的研发、生产和检验能力;
(2)应当设立独立的特殊医学用途配方食品研发机构,并配备专职人员和设备;
(3)执行《特殊医学用途配方食品良好生产规范》(GB29923-2013);
(4)执行《食品安全管理体系食品链中各类组织的要求》(GB/T22000-2006);
(5)具有标准规定的全部项目检验能力。
详解注册办法
【一、注册机构】
国家食品药品监督管理总局食品审评机构负责特殊医学用途配方食品注册的审评工作。
【二、注册流程】
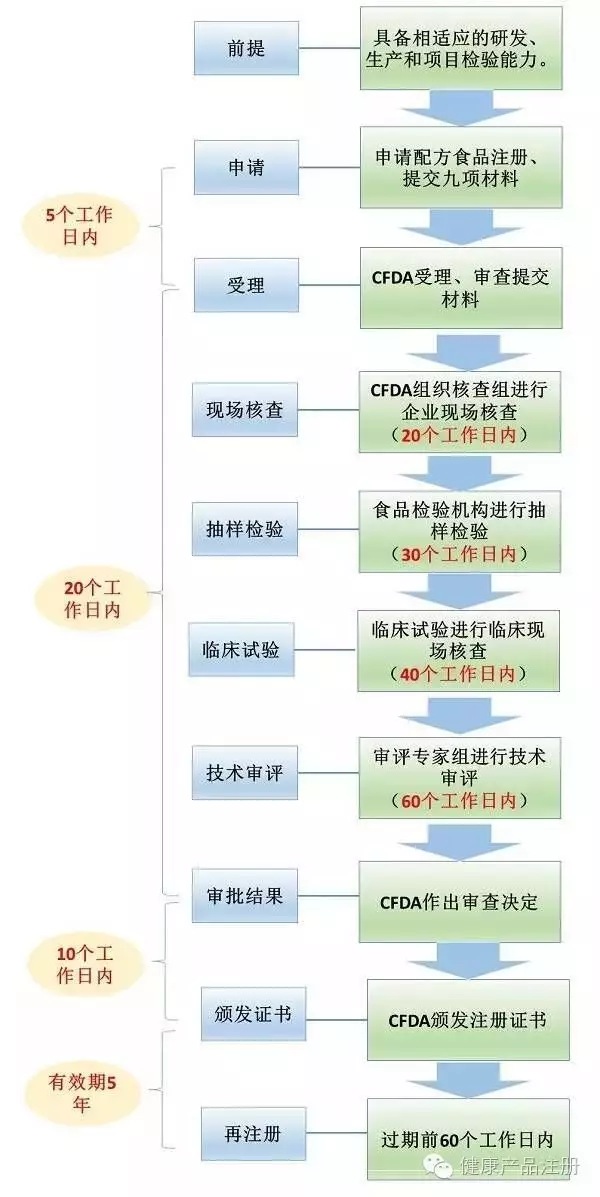
【三、注册范围】

【四、申请材料】
(一)特殊医学用途配方食品注册申请书;
(二)产品研发报告和产品配方设计及依据;
(三)生产工艺资料;
(四)产品质量的标准要求;
(五)产品标签、说明书设计样稿;
(六)试验样品检验报告;
(七)研发、生产和检验能力证明材料;
(八)其他表明产品安全性、营养充足性的材料;
(九)特定全营养配方食品注册,还应提交临床试验报告。
【五、证书内容】
(一)产品名称
(二)企业名称、法定代表人、生产地址
(三)注册号及有效期
(四)产品类别
(五)产品配方
(六)生产工艺
(七)产品标签、说明书
【六、再注册】
特殊医学用途配方食品注册证书有效期为5年。有效期届满,需要继续生产或进口的,应当在有效期届满60日前,向国家食品药品监督管理总局提出再注册申请,并提交下列材料:
(一)特殊医学用途配方食品再注册申请书;
(二)特殊医学用途配方食品注册证书;
(三)5年内产品生产、销售、监督抽检情况,对产品不合格情况应当做出说明;
(四)5年内产品使用情况及不良反应情况总结。
【七、不予再注册的情况】
(一)注册后未取得生产许可的;
(二)未在规定时间内提出再注册申请的;
(三)注册产品一年内在省级以上监督抽检中出现2次及以上不合格的;
(四)企业未能保持生产、研发、检验能力的;
(五)企业未按要求记录生产销售信息的;
(六)其他不符合有关规定的情形。
