北京中健天行医药具有20年的保健食品研发、生产经验,可为企业提供权威的技术研发,包括产品配方、工艺以及技术要求,资深评审专家把关,研究数据详实、规范、可追溯,有效保障产品注册申报和商业化生产。
一、配方研究
1.安全
①原料和辅料的使用依据
应按照普通食品(包括可用于普通食品的物品、食品添加剂,下同)、新食品原料、“按照传统既是食品又是中药材的物质”、“拟纳入保健食品原料目录”以及保健食品新原料等类别,明确原辅料的使用依据。
使用保健食品新原料的,应参照新食品原料安全性审查的有关规定,提供保健食品新原料的研制报告、国内外的研究利用情况等安全性评估材料和毒理学试验报告、生产工艺、质量要求、检验报告。
②产品配方配伍及用量的安全性科学依据
应从传统配伍禁忌和现代医学药理学研究方面,提供产品配方配伍及用量理论依据、文献依据和试验数据等科学依据。提供配方原料的品种、等级、质量、用量及个数符合有关规定的依据。
2.功能
①配方主要原料具有功能作用的科学依据,其余原料的配伍必要性
产品配方原料应具有明确的使用目的。应提供配方主要原料具有功能作用的科学依据,并阐明其余原料的配伍必要性。
以经简单加工的普通食品为原料的,应提供充足的国内外实验性科学文献依据,重点明确所用原料的功效成分和含量以及量效关系。
②产品配方配伍及用量具有保健功能的科学依据
应提供产品组方原理、产品配方配伍及用量具有声称功能的理论依据及文献依据等。
二、工艺研究
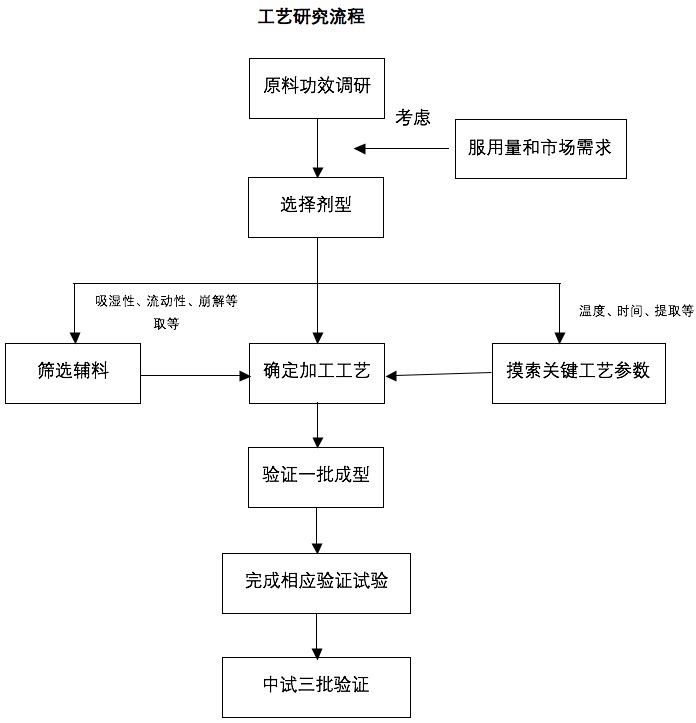
设计合适的处方、摸索适合的加工剂型、工序和关键工艺参数、选择合适的包装材料是工艺研究的主要内容。
三、方法研究
根据产品检测方法来源,应提交产品标志性成分或功效成分检测方法学研究资料,明确检测方法建立的研究过程,验证检测方法的准确性、重现性和适用性。还应按《保健食品注册申请服务指南》(以下简称《指南》),提交研究人员、研究时间、研究地点等溯源性资料。属委托研究的,还应提交委托研究合同(协议)等。
(一)引用国家相关标准方法的,考虑方法建立时已进行方法学研究,不要求提供检测方法建立的研究资料,但应参照GB/T 5009.1《食品卫生检验方法 理化部分 总则》,考察检出限、精密度、准确度、线性范围。
(二)检测方法对国家相关标准方法的样品前处理、检测条件等内容进行修订的,重点对方法修订部分进行方法学研究,提供研究资料,并参照GB/T 5009.1《食品卫生检验方法 理化部分 总则》,考察方法的检出限、精密度、准确度、线性范围。
(三)申请人自行制订检测方法的,应提供全部的方法学建立研究报告,参照GB/T 5009.1《食品卫生检验方法 理化部分 总则》,考察检出限、精密度、准确度、线性范围,并考察所建立方法的专属性与耐用性。
