2025保健食品备案榜单揭晓!冠军企业狂揽126款,山东成最大赢家!
2026-01-04
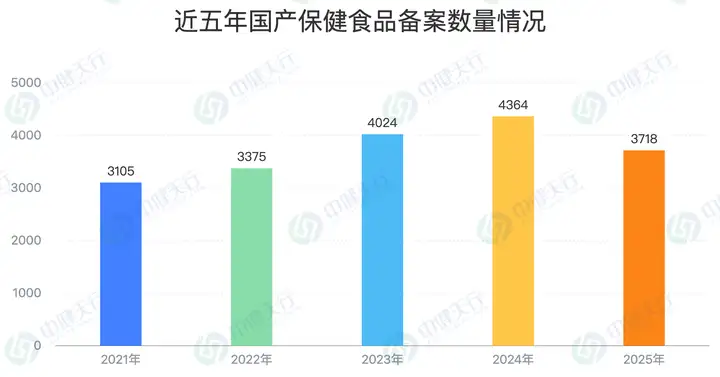
2025年,我国保健食品行业注册备案双轨制持续深化,备案通道已成为市场准入的主流路径。据国家市场监督管理总局公开数据显示,2025年全年新增备案保健食品3744款,含国产3718款,进口26款。本文基于上述权威数据,全面复盘2025年保健食品备案整体情况,为行业发展提供数据支撑与决策参考。
1.保健食品备案数量情况
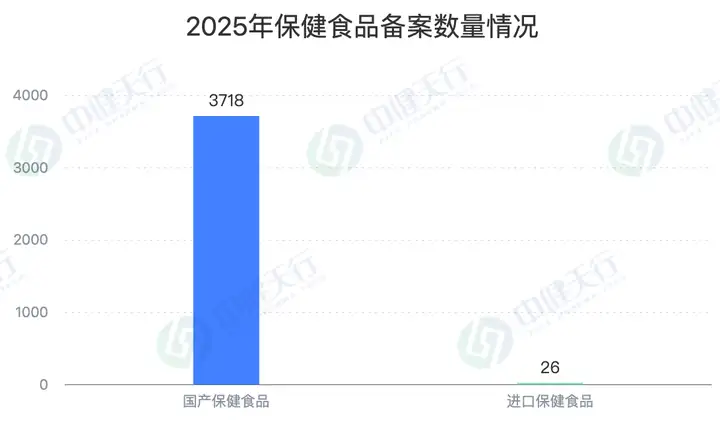
截至2025年12月31日,国家市场监督管理总局共公布3744个保健食品备案信息。从市场主体构成来看,国产与进口产品呈现“一边倒”格局:国产备案产品3718个,占比高达99.3%;进口备案产品仅26个,占比不足1%,反映出国内供应链在备案通道的适配性与便捷性上具有显著优势。
2.不同国家地区备案数量情况
01.国产保健食品
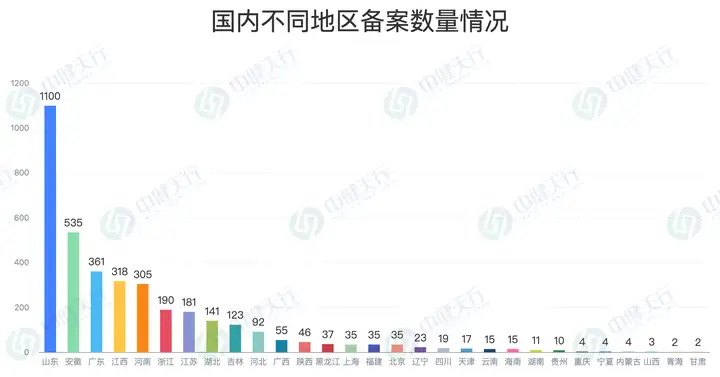
2025年国产保健食品备案呈现明显的区域集聚特征。从全年数据来看,山东省(1100个)以绝对优势位居备案数量首位;安徽省(535个)、广东省(361个)紧随其后。
在2025年备案凭证数量最多的企业中,威海百合生物技术股份有限公司表现抢眼,共有126款保健食品成功获得备案凭证,位居榜首。山东健康源生物工程有限公司紧随其后,以121款备案凭证数量位列次席,好棣(山东)生物科技有限公司则以62款备案凭证数量取得第三的位置。
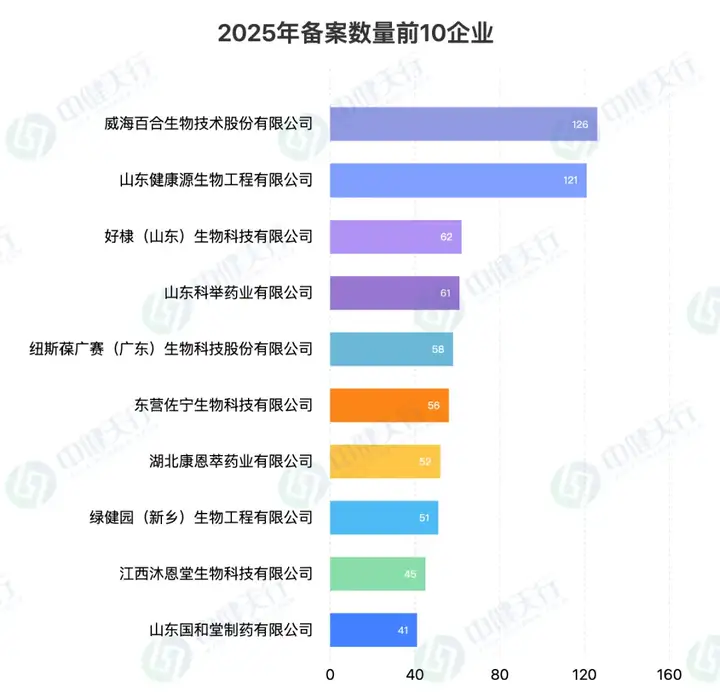
02.进口保健食品
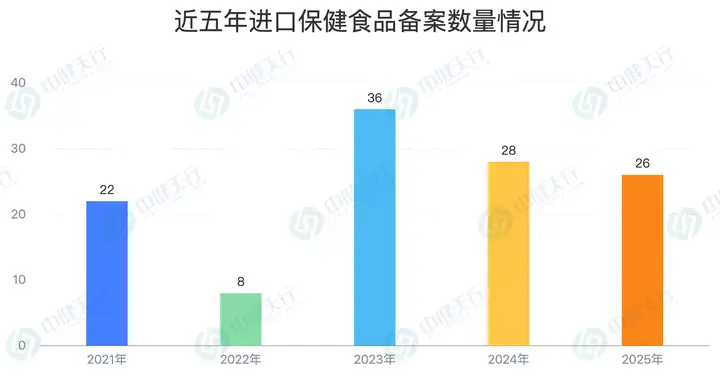
2025年,共有11家企业的26款进口保健食品获得备案凭证,这些产品分别来自美国、日本、澳大利亚、德国、加拿大等七个国家和地区。
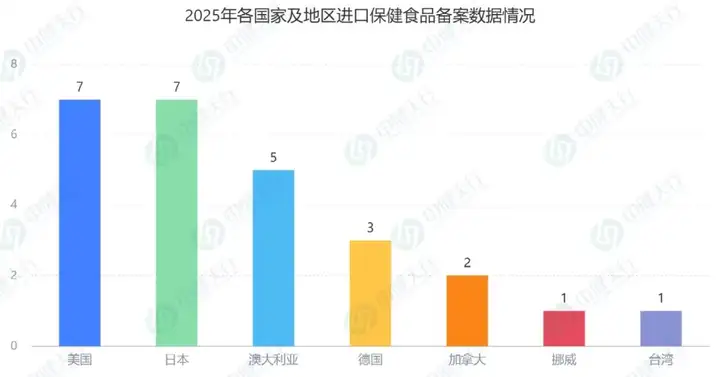
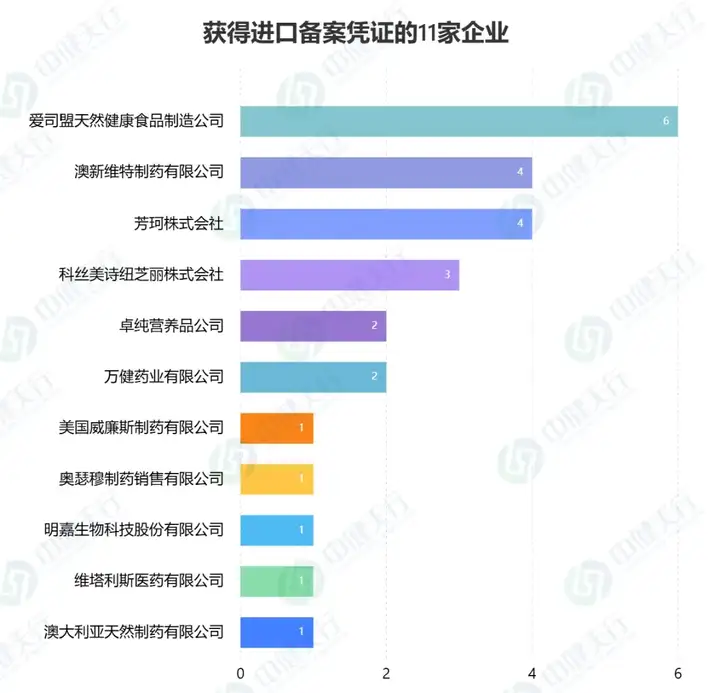
3.不同剂型备案情况
2025年备案产品的剂型分布高度集中,片剂(1185个)、软胶囊(775个)、粉剂(660个)三大剂型合计占比达70%,成为市场主流。剂型选择的集中化,核心源于消费者对“便捷性”的需求——胶囊与片剂便于携带、服用剂量精准,且生产工艺成熟、质量可控性强,能够有效降低企业的研发与生产风险。此外,口服液作为第三大剂型,主要适配儿童、老年人等特殊人群的服用需求,填补了细分市场空白。
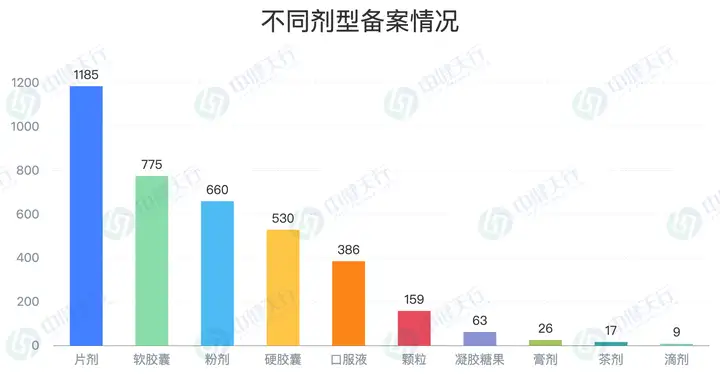
4.不同功效成分备案情况
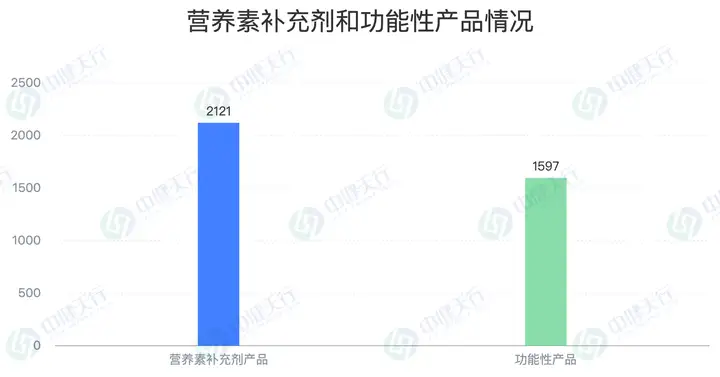
2025年国产备案产品中,营养素补充剂产品2121个,功能性产品1597个,两者数量基本相当、占比接近1:1,标志着备案市场从早期以基础营养素为主,逐步转向基础营养与功能性产品协同发展的均衡格局。这一变化与消费者健康需求的多元化升级密切相关:基础营养素满足大众日常营养补充需求,而非营养素补充剂则聚焦特定健康诉求,形成差异化市场供给。
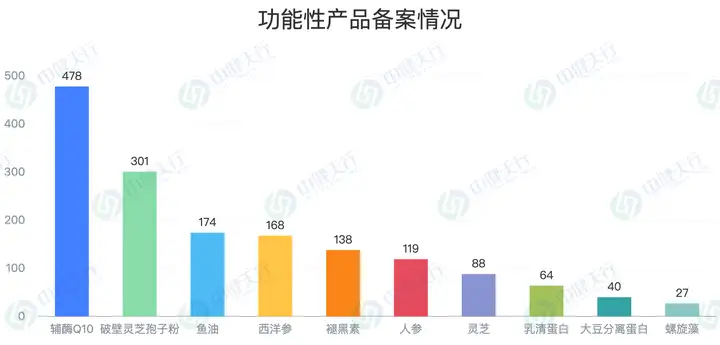
细分品类中,功能性产品集中度较高。辅酶Q10(478个)、破壁灵芝孢子粉(301个)、鱼油(174个)占据前三甲,合计占功能性产品的61.5%;西洋参(168个)、褪黑素(138个)、人参(119个)等经典成分保持稳定需求,成为企业备案的“热门选择”。这一现象既反映出市场对成熟成分的认可度较高,也体现了企业在合规前提下规避创新风险的理性策略。
2025年,我国保健食品备案市场呈现出“总量增长、结构均衡、区域集聚、政策赋能”的良好态势。备案制作为市场准入主渠道的地位进一步巩固,国产产品凭借供应链与合规优势占据绝对主导,经典成分与便捷剂型成为市场主流,委托生产等精细化分工模式推动产业效率提升。政策层面的审评审批优化与复方配伍试点,既降低了企业合规成本,又拓展了产业创新空间,为行业高质量发展奠定了坚实基础。
展望未来,随着复方配伍备案试点的逐步推进,中医药特色保健食品将成为新的增长亮点;进口备案市场在跨境电商政策规范的推动下,有望逐步突破合规瓶颈。对于企业而言,把握政策导向、聚焦消费者真实需求、强化合规能力与供应链优势,将是在备案市场竞争中脱颖而出的核心关键。
