NMN禁令美国裁决延迟,中国公司领跑欧盟审批
2025-08-22
2025年7月29日,美国天然产品协会(NPA)在其官网发布最新NMN诉讼进展报告显示,由于FDA于2025年4月启动大裁员,限制了相关人员处理本项目的时间精力,FDA对NPA的请愿回应时间预计将延后至2025年9月30日。这意味着至少在9月30日前,NMN在美国仍可合法销售!

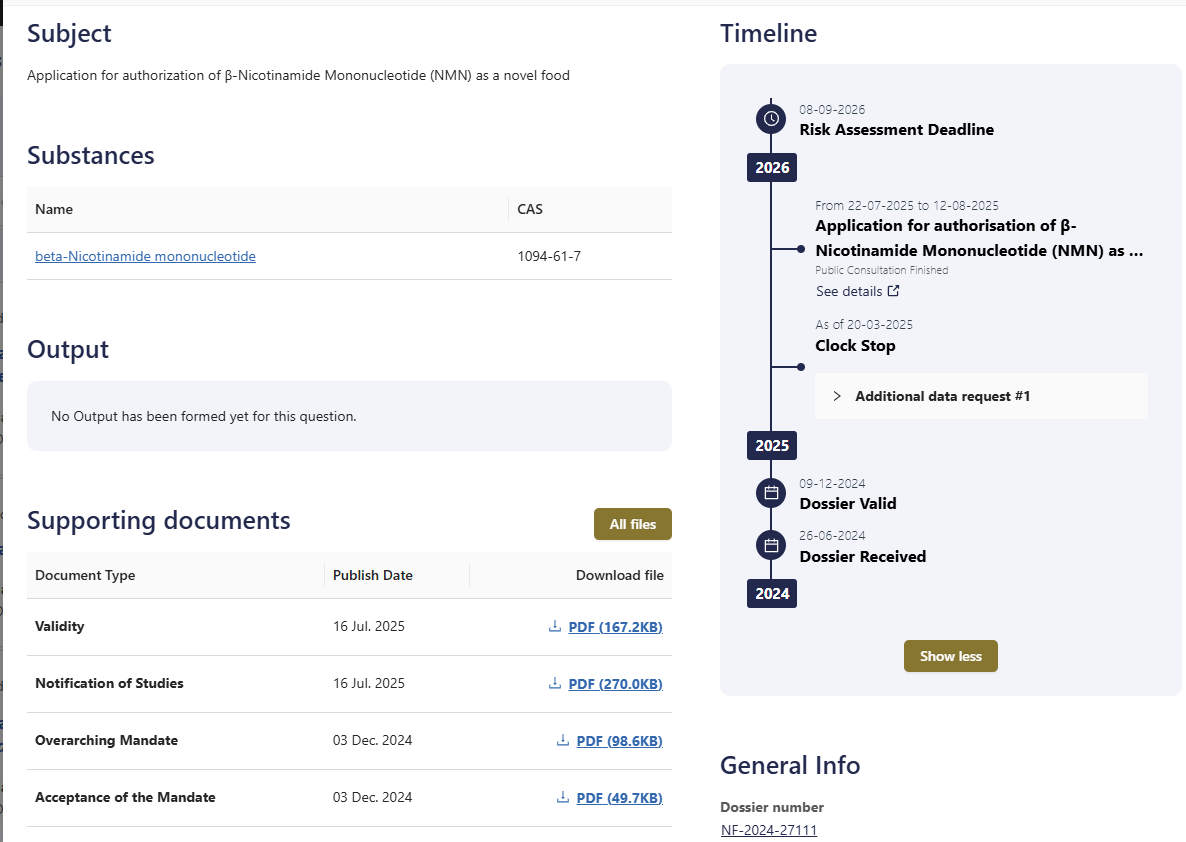
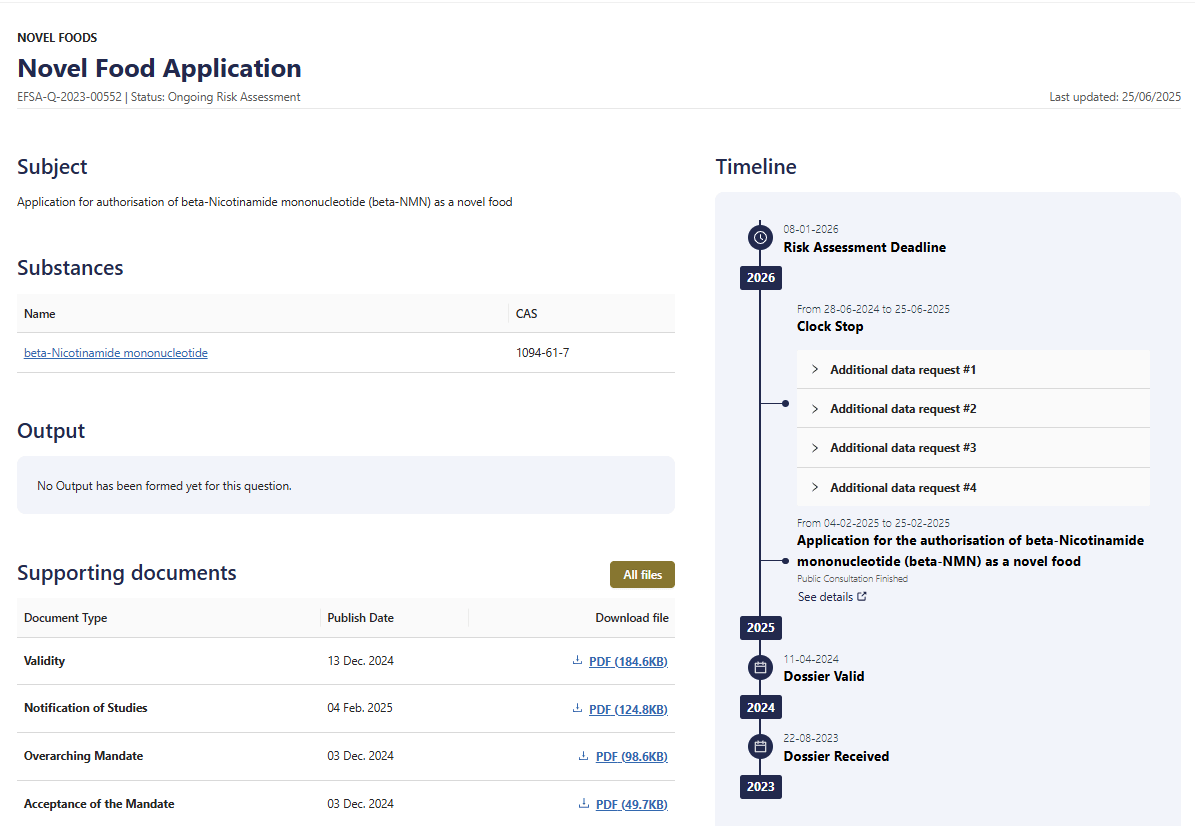
虽然NMN在美国的合规之路尚在探索,但在欧盟的合规进程有序推进,欧盟已收到5款NMN的新型食品(Novel Food)申报,其中音芙医药(EffePharm)、尚科生物两家中国企业的申报已进入欧洲食品安全局(EFSA)的安全性评估阶段,有望打破其全球合规僵局。其中,音芙医药(EffePharm)旗下Uthever NMN于2025年2月完成EFSA公众咨询,成为全球首个进入最终审查阶段的NMN原料。
全球监管格局:NMN的全球 regulatory landscape 呈现显著差异
欧盟:严格遵循“预防原则”,需通过EFSA全面安全评估方可上市,目前尚无获批案例;
中国:2023年5月明确NMN不得作为食品原料,跨境电商渠道亦于2024年6月受限,陆续有相关NMN添加剂、新食品原料申请,但都未批准;
美国:FDA因NMN作为药物临床试验物质(如MetroBiotech的MIB-626)暂停其膳食补充剂身份,2024年11月联邦法院裁定暂缓执行禁令;
日本:2020年将NMN纳入“非药品成分清单”,允许无剂量限制使用,成为全球首个开放NMN食品应用的国家。
EFSA启动评估,被业内视为NMN从“争议成分”向“主流原料”转型的关键信号。EFSA预计将于2026年第一季度发布科学意见,欧盟委员会将在随后6个月内作出最终授权决定。届时,NMN能否成为首个“欧盟认证抗衰原料”,值得全球行业关注。若尚科生物与音芙医药的申请均获通过,将推动NMN全球化发展。
新食品原料申报的成功,离不开资料规范与全流程把控。近年审批效率提升,但因预评估不足、资料不当等导致的延期、不予许可仍频发。在国家卫健委公布的新食品原料及实质等同名单中,北京中健天行医药凭借多款产品获批的成绩,在行业内积累了极为丰富的成功申报经验,项目实力名列前茅。我们可为申报的新食品原料提供全面评估与分析,量身定制经济、可行且有保障的申报方案。欢迎相关申报企业来电交流!

