新食品原料管理现状及申报解析
2017-01-05
一、新食品原料管理进展情况
新食品管理历史沿革--法律
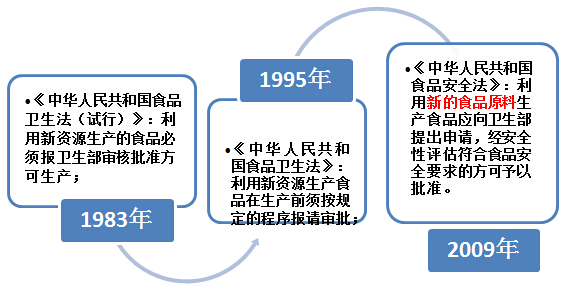
新食品管理历史沿革--法规
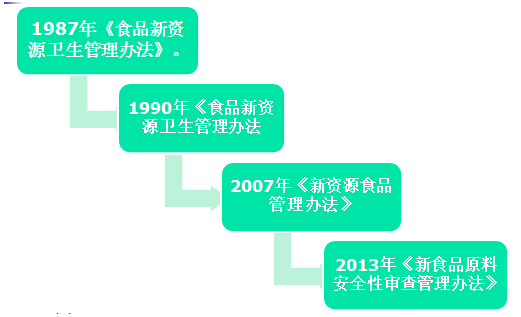
新食品管理历史沿革--管理思路变迁

新食品原料管理历史沿革--内容变化
|
《食品新资源卫生管理办法》(1990) |
《新资源食品管理办法》(2007) |
《新食品原料管理办法》(2013) |
|
三新(新发现、新研制、新引进) |
四个范围:动物、植物微生物;提取物;加工用微生物新品种;新工艺结构改变。 |
四个范围:动物、植物、微生物;提取物;原有结构发生改变的食品原料 |
|
终产品或食品原料 |
食品原料 |
食品原料 |
|
审核批准后向申报企业颁发批件 |
审核批准后 向社会公告 |
审核批准后 向社会公告 |
二、新食品原料安全性审查管理办法解读
《办法》及其配套实施文件
《新食品原料安全性审查管理办法》:2013年5月31日国家卫生与计划生育委员会第1号主任令发布,并将于2013年10月1日实施。配套实施文件已经发布实施:10月15日国卫食品发〔2013〕23号“国家卫生计生委关于印发《新食品原料申报与受理规定》和《新食品原料安全性审查规程》的通知”。
依据
根据《食品安全法》第四十四条:利用新的食品原料生产食品应当取得许可;
《食品安全法实施条例》第二十五条:企业采购食品原料应提供产品合格证明文件。
《行政许可法》及《卫生行政许可管理办法》:公平、公正、公开、效率、便民五大原则
定义
(1)在我国无传统食用习惯的动物、植物和微生物;
(2)从动物、植物和微生物中分离的成分;
(3)食品成分的原有结构发生改变的;
(4)其他新研制的食品原料。
释义:一是将食品加工过程中使用的微生物新品种纳入第一类管理,二是增加了合成类等其他新研制食品原料。
承担部门及机构
卫计委负责新食品原料安全性评估材料的审查和许可工作;
卫生监督中心承担新食品原料安全性评估材料的申报受理、组织开展安全性评估材料的审查等工作。
网上申报
第九条:申请人提交材料时,应注明不涉及商业秘密可以向社会公开的内容。
释义:除了申请表外,下列下列需向社会公开:包括研制报告、安全性评估报告、生产工艺、执行的相关标准、标签说明书。
监督中心已经完善了网上受理评审系统,企业网上提交后,一经受理即可向社会公开。
征求意见
第十条:国家卫生计生委受理新食品原料后,向社会公开征求意见。
释义:增加了受理后即向社会征求意见的程序。在不涉及企业商业机密的前提下,受理之后即向社会公开征求意见。
充分体现一家申报、多家受益,减少审批。
众多企业提前介入,可以充实完善公告内容!
审查时间和专家组成
卫计委受理新食品原料申请之日起60日内,应当组织专家对新食品原料安全性评估材料进行审查,并作出审查结论。
专家组成:按照食品安全法,由医学、农业、食品、药学等方面专家。按照专业分类:毒理、卫生学、工艺、标准、标签。
现场核查
审查过程中需要对生产工艺进行现场核查的,审评机构可以组织专家对新食品原料研制及生产现场进行核查,并出具现场核查意见。
专家对所出具的现场核查意见负责。
省级卫生监督机构配合实施。
参加现场核查的专家不再参加该产品审查表决。
补充资料
审查过程中需要补充资料的,书面告知申请人,申请人按照要求及时补充资料。
解读:专家审查认为该产品按照要求补充资料后可以批准的产品,才会做出补充资料延期再审的决定。
申请人在一年内按照提交书面补充资料,符合要求的予以批准,不符合要求的,可以继续补充,也可能不批准。
现场答辩
根据审查工作需要,可以要求申请人现场解答有关技术问题,申请人应当予以配合。
解读:在操作上是由监督中心提前一周给申请人电话,告知现场答辩的时间、地点和内容。答辩时间为15分钟,介绍10分钟,专家提问5分钟。一般情况下申请人自愿参加。
审查决定
卫计委根据专家的安全性审查结论,对符合食品安全要求的,准予许可并予以公告;对不符合食品安全要求的,不予许可并书面说明理由。
释义:说明不批准理由,还要告知行政复议和诉讼的权利。
对与食品或者公告的新食品原料具有实质等同性的,应当作出终止审批的决定,并书面告知申请人。
释义:文书相当于证明文件。
关于实质等同
实质等同定义:与食品或者已经公布的新食品原料在种属、来源、生物学特征、主要成分、使用部位、使用量、使用范围和应用人群等方面相同,所采用的工艺和质量要求基本一致,可以视为同等安全。
判定主体改变:删除了原来由企业自行认定条款。
释义:企业自行认定实质等同规定形同虚设,各方监管不予认可:QS认证、企业标准备案、进口审查、保健食品注册…
公告内容
(一)名称;
(二)来源;
(三)生产工艺;
(四)主要成分;
(五)质量规格要求;
(六)标签标识要求;
(七)其他需要公告的内容。
释义:不同性质的原料,其公告内容不同,动植物类:名称、来源提取物类:质量规格;微生物类:菌株号。有特殊要求的:使用人群、警示标识等。
标签要求
标签:食品中含有新食品原料的,其产品标签标识应当符合国家法律、法规、食品安全标准和卫生部公告要求。
释义:符合预包装食品标签要求。对于新原料的包装标签必须标准不适宜人群和警示用语。对于含该新原料的食品没有要求。
再评估
有下列情形之一的,卫计委应及时组织对已公布的新食品原料进行重新审查:
1、随着科学技术的发展,对新食品原料安全性产生质疑的;
2、有证据表明新食品原料的安全性可能存在问题的;
其他需要重新审查的情形。
对重新审查不符合食品安全要求的新食品原料,卫计委可以撤销许可。
法律责任
申请人责任:应当如实提交有关材料,反映真实情况,对申请材料内容的真实性负责,并承担法律责任。
释义:提供虚假材料者,按照《行政许可法》有关规定,不予许可,且一年内不得再次申请许可。
企业责任:违反本办法规定生产或使用未经安全性评估的新食品原料的,按照《食品安全法》有关规定处理。
释义:食品安全法第八十五条利用未经安全性评估的新原料从事食品生产的,处以没收违法所得、罚款以及吊销许可的处罚。
配套文件:修订《新食品原料申报与受理规定》
《新食品原料申报与受理规定》(26条)
增加了不属于申报的情形
以下情形不属于新食品原料的申报范围:
(一)不具有食品原料特性;
(二)已列入食品安全国家标准《食品添加剂使用标准》(GB2760)、《食品营养强化剂使用标准》(GB14880)的;
(三)国家卫生计生委已作出不予行政许可决定的;
(四)其他不符合有关法律、法规规定和新食品原料管理要求的。
配套文件:制定《新食品原料安全性审查规程》
新食品原料申报要完成成分分析、卫生学、毒理学安全性评价、风险性评估意见等报告,历经企业答辩、专家评审、补正资料甚至现场核查以及公开征求意见等程序,申报材料要求和审核程序非常严格和复杂,成功与否与申报资料标准、规范的准备密切相关,应在申报之前进行预评估,以避免出现多次延期审查以及不予行政许可的情况。在国家卫健委公布的新食品原料及实质等同名单中,北京中健天行医药有多款产品获批,有丰富的成功申报经验,会对申报的新食品原料进行全面评估及分析,提供经济、可行、保障的申报方案,欢迎申报企业来电与我们交流!

